GSP 301 NS是一种新型的抗组胺药和皮质类固醇的复方鼻喷剂,该产品已在美国、澳大利亚、韩国、俄罗斯、英国及欧盟等多个国家和地区获批上市销售;
本次研究是一项随机、双盲、双模拟、三臂、多中心、平行对照的III期临床研究,共入组535名12岁及以上季节性过敏性鼻炎(SAR)患者,旨在评估GSP 301 NS治疗的有效性、安全性、耐受性及药代动力学特征;
根据《过敏性鼻炎及其对哮喘的影响(ARIA)》指南,鼻用抗组胺药和鼻用皮质类固醇药是SAR的首选用药,对于中、重度SAR患者,建议联合使用鼻用抗组胺药和鼻用皮质类固醇药。
近日,远大医药(0512.HK)全球创新产品Ryaltris®复方鼻喷剂(GSP 301 NS)在中国开展的用于治疗12岁及以上患者的季节性过敏性鼻炎(SAR)的III期临床研究(GSP 301-308)已完成并成功达到主要终点,这是本集团在呼吸及重症抗感染板块的又一项重要研发进展。
GSP 301 NS临床数据优势显著 已在海外多地获批上市
关于GSP 301-308
该研究是一项随机、双盲、双模拟、三臂、多中心、平行对照的III期临床研究,共入组了535名12岁及以上SAR患者,以1:1:1的比例被随机分配至GSP 301 NS治疗组以及两个原研单方阳性对照药治疗组——盐酸奥洛他定鼻喷剂(Patanase NS)和糠酸莫米松鼻喷剂(内舒拿®NS),均给药14天并收集患者对用药后症状改善的评分信息,以评估GSP 301 NS治疗的有效性、安全性、耐受性及药代动力学特征。
GSP 301-308疗效评价采用了国际上公认的反射性鼻部症状总评分(rTNSS)与瞬时鼻部症状总评分(iTNSS)评分表。评分表中评分值越高表明患者鼻部症状越严重,用药后评分下降表明患者症状有所改善,评分值较基线值(用药前评分值)变化越大表明患者接受治疗后SAR症状改善越明显。
此临床研究疗效性的主要观察终点为:GSP 301 NS治疗组14天期间受试者自评的上午和下午12小时rTNSS平均值较基线的变化值,与两种单方阳性对照药治疗组的变化值进行比较。若试验用药组较对照组下降更多,说明试验用药疗效更明显。
本研究的临床结果显示,GSP 301 NS组、Patanase NS组和内舒拿®NS组治疗14天期间受试者自评的上午和下午12小时rTNSS平均值较基线变化的最小二乘均值分别为-3.84、-2.58和-3.35。由统计数据可见,GSP 301 NS组rTNSS下降幅度大于Patanase NS组和内舒拿®NS组,且组间差异有临床意义和统计学意义(GSP 301 NS vs. Patanase NS, P<0.0001; GSP 301 NS vs.内舒拿®NS, P=0.0018),证明GSP 301 NS的疗效评分均优于单方原研制剂Patanase NS和内舒拿®NS。同时,产品的安全性、耐受性及药代动力学特征也都达到了预设的临床终点。
关于GSP 301 NS
GSP 301 NS是一种新型的抗组胺药和皮质类固醇的复方鼻喷剂,用于治疗成人和青少年的SAR。作为复方制剂,GSP 301 NS能够给SAR患者带来更为便捷的治疗方式,提高患者的依从性,为SAR患者带来新的治疗手段。该产品于2022年1月获美国食品药品监督管理局(FDA)批准上市,在此之前已在澳洲、韩国、俄罗斯、英国和欧盟等多个国家和地区获批上市销售。GSP 301 NS于2021年10月获国家药监局批准开展III期临床试验,于2022年4月完成首例受试者入组,于2023年5月完成全部受试者入组,GSP 301-308为GSP 301 NS在中国的注册性临床研究,研究的顺利完成是该项目在中国落地工作的又一个重要里程碑。
关于过敏性鼻炎
中国是世界上过敏性鼻炎发病率最高的国家之一。根据中国相关流行病学调查结果,中国成人过敏性鼻炎患病率约17.6%,患病群体已近2.5亿人口,其中中-重度持续性过敏性鼻炎患者约1.3亿,患者群体庞大。根据《过敏性鼻炎及其对哮喘的影响(ARIA)》指南,鼻用抗组胺药和鼻用皮质类固醇药是SAR的首选用药,对于中、重度SAR患者,建议联合使用鼻用抗组胺药和鼻用皮质类固醇药,而目前中国国内的鼻用制剂主要以单方制剂为主,临床需求迫切,市场前景巨大。
持续推进创新产品研发 深化呼吸及重症抗感染板块布局
呼吸及重症抗感染板块为本集团核心战略板块之一,该板块在售产品超过10款,覆盖鼻炎、咽炎、支气管炎、肺炎、哮喘等多个适应症,在呼吸疾病治疗领域已形成了较为完备的产品组合。其中,该板块核心产品切诺、金嗓系列、恩明润®比斯海乐®和恩卓润®比斯海乐®均为全国独家品种,诺通、力美松、抗病毒口服液等多个产品均处于细分领域的领先地位。
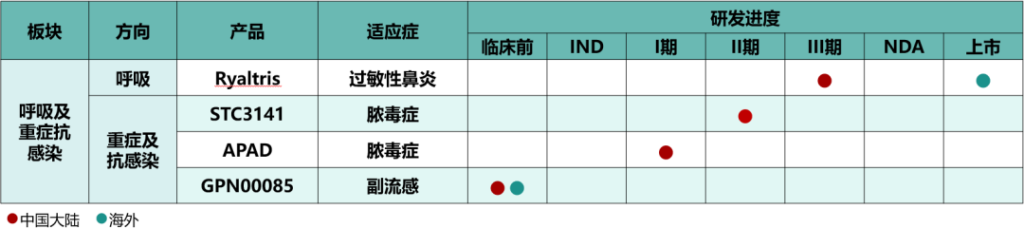
在研产品方面,本集团针对未被满足的重大临床需求进行创新布局,已有多款在研创新产品覆盖过敏性鼻炎、脓毒症、急性呼吸窘迫综合征(ARDS)、副流感、新冠病毒感染(COVID-19)等。其中,用于治疗脓毒症等重症的全球创新药物STC3141已在五个国家和地区获得七个临床批件,完成了三项针对患者的临床研究,在中国开展的针对ARDS的Ib期临床研究、在欧洲开展的针对重症病毒感染的IIa期临床研究,以及在澳洲和比利时开展的针对脓毒症的Ib期临床研究均已达到临床终点;在中国已获批开展用于治疗脓毒症的II期临床研究。另一款用于治疗脓毒症的全球创新产品APAD已获批开展I期临床研究并完成首例患者入组。
在该板块的重症及抗感染方向,本集团立足于糖组学研发技术平台,在澳洲设立了研发中心进行全球创新产品的开发工作。本集团澳洲研发中心与澳洲国立大学及澳洲格里菲斯大学保持长期深度合作,持续开发全球创新技术产品和治疗方法。其中,副流感项目是与“扎那米韦”发明人、澳洲格里菲斯大学糖组学研究所所长进行合作,该研究所是全球少数专注糖组学的科研机构之一,也是该领域中全球最大的科研机构之一。
未来,本集团将继续采用自主研发与全球拓展的研发理念,打造气道慢病全周期管理产品集群和重症抗感染产品管线,不断巩固本集团在该领域的行业地位。
远大医药集团有限公司董事会表示:
本集团一直高度重视创新产品和先进技术的研发,未来将持续加大对全球创新产品和先进技术的投入,丰富和完善产品管线及产业布局,坚持“全球化运营布局,双循环经营发展”策略,充分发挥本集团的产业优势和研发实力,快速将科技创新产品落地上市,为全球患者提供更先进更多样的治疗方案。





