- OC-01于2021年10月在美国获批上市,是目前全球首款且唯一一款获批增加干眼症患者泪液分泌的无防腐剂、多剂量、无菌包装鼻喷雾剂[1];
- OC-01是高选择性的烟碱乙酰胆碱受体激动剂,可通过启动三叉神经副交感神经通路,增加基础泪液的分泌,从而有望实现增加干眼症患者的泪液分泌;
- OC-01一天仅需两次鼻喷给药,可避免传统滴眼药使用的繁琐性,有望提高患者的依从性,有望为干眼症患者提供一种耐受性良好且疗效确切的全新治疗选择。
近日,远大医药(0512.HK)全球首创用于增加干眼症患者泪液分泌的鼻喷产品酒石酸伐尼克兰鼻喷雾剂(OC-01),在正式获批后于中山大学附属第一医院和深圳市眼科医院实现中国大陆首批商业化处方落地。这一里程碑进展标志着中国干眼症治疗迎来全新选择:中国目前唯一一款获批上市的用于增加干眼症患者泪液分泌的鼻喷产品正式投入临床应用[1],为中国干眼症患者提供一种全新的治疗方案。
OC-01创新经鼻给药 或提供干眼症全新治疗选择
关于OC-01
OC-01是高选择性的烟碱乙酰胆碱受体激动剂,普遍认为可通过启动三叉神经副交感神经通路,增加基础泪液的分泌,从而增加干眼症患者的泪液分泌。该产品于2021年10月在美国获批上市,是目前全球首款且唯一一款获批治疗患者干眼症症状的鼻喷雾剂[1];中国大陆方面,该产品于2024年11月获得国家药监局批准上市;此外,OC-01于2023年2月在中国澳门特别行政区获批上市;于2023年4月作为进口临床急需药品,落地海南乐城医疗先行区;于2024年11月在中国台湾地区获批上市。
关于干眼症及其治疗
干眼症为临床常见的慢性眼表疾病,中国干眼症发病率大约在21%-30%,干眼症患者人群保守估计约3.6亿人。目前,医疗机构门诊就诊的干眼症患者占眼科总就诊人数的30%以上,预计未来5-10年,该比例可能会上升到40%,干眼症已成为影响国民健康的重要社会公共卫生问题。最常用的治疗方案为人工泪液,但天然泪液成分较为复杂,含有上千种成分,而目前已上市的人工泪液产品仅可仿真泪膜的单一或部分成分,难以真正做到天然泪液的替代;此外,市面上常见的人工泪眼产品多为眼表滴注的给药方式,需要频繁给药,存在长期药物刺激风险,影响患者依从性。因此,人工泪液的治疗效果存在较大的个体差异。OC-01采用创新的经鼻给药方式,显著改善了干眼症患者的天然泪液分泌量,提高泪膜稳定性,阻断干眼病理生理的恶性循环。同时,OC-01一天仅需两次鼻喷给药,使用方便,可避免传统滴眼药使用的繁琐性,有望提高患者的依从性。该产品有望为干眼症患者提供一种耐受性良好且疗效确切的全新治疗选择。[2]
推进全球创新产品研发 夯实眼科领域行业地位
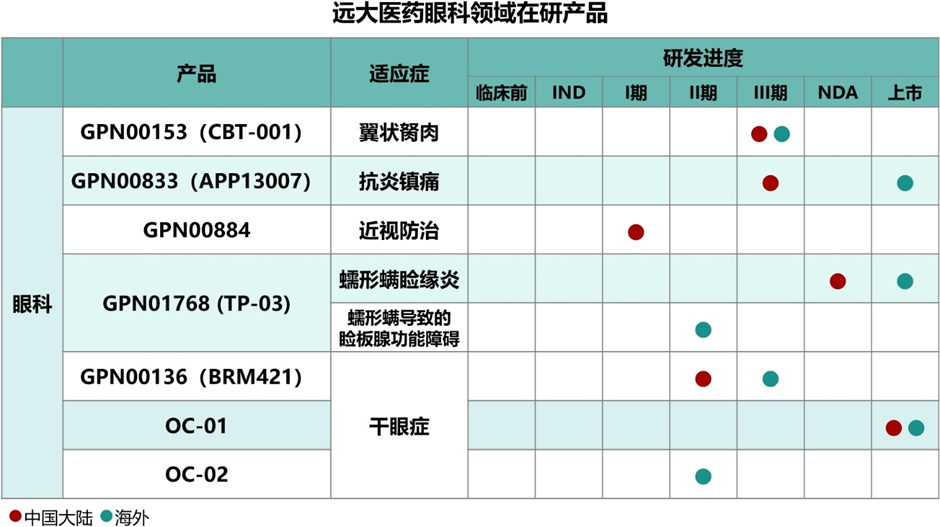
本集团始终以眼科领域作为重要战略发展方向之一,持续聚焦眼科药物创新,坚持专业化发展道路,不断提升行业地位和市场竞争力。目前,本集团已构建“专业化、全系列、多品种”的创新药物产品体系,储备了治疗“近视”、“干眼症”、“翼状胬肉”、“眼科术后抗炎镇痛”、“蠕形螨睑缘炎”和“蠕形螨导致的睑板腺功能障碍”的多款全球创新产品,且取得了重大研发进展,未来三年将有多款创新产品有望获批上市。[3]
其中,用于治疗蠕形螨睑缘炎的全球创新眼科药物GPN01768 (TP-03,洛替拉纳滴眼液,0.25%)已于2024年12月向药监局递交了新药上市申请并获得了受理,于2025年5月获得中国澳门特别行政区政府药物监督管理局批准上市;用于抗炎镇痛的激素纳米混悬滴眼液GPN00833于2024年11月完成国内III期临床研究并达到了临床终点;用于治疗翼状胬肉的创新改良型新药GPN00153 (CBT-001)于2024年3月完成中国III期临床研究首例患者入组,于2025年6月完成国际多中心III期临床研究全球中心全部患者入组;用于推迟儿童近视进展的全球创新眼科药物GPN00884于2024年6月完成中国I期临床研究首例患者入组给药。[3]未来,本集团将加快推进研发管线的全面化、差异化布局,不断丰富眼科细分领域的创新产品储备。此外,本集团在眼科领域已吸引和培养了一批兼具临床经验和营销经验的专业人士,建立了以客户为中心,学术为主导的专业化营销团队,并与大型医药流通企业和连锁药店建立了长期稳定合作,形成了覆盖全国的营销网络。随着眼科创新产品的持续获批,本集团将充分发挥该领域的核心优势,持续深耕眼科前沿创新赛道,进一步加强核心产品的专业化推广和品牌建设,为本集团持续健康发展提供新动能。
远大医药集团有限公司董事会表示:
本集团一直高度重视创新产品和先进技术的研发,未来将持续加大对全球创新产品和先进技术的投入,丰富和完善产品管线及产业布局,坚持‘全球化运营布局,双循环经营发展’策略,充分发挥本集团的产业优势和研发实力,快速将科技创新产品落地上市,为全球患者提供更先进更多样的治疗方案。
[1]根据现有公开信息;
[2]根据产品III期临床试验数据,具体疗效因人而异;[3]研发风险提示:文中提及的在研产品尚未获得上市批准,其安全性和有效性需经完整临床研究及监管审批确认,不构成任何治疗承诺或商业推广。





